2.3. Определение содержания нитратов в почве по Грандваль- Ляжу
Метод основан на взаимодействии нитратов с дисульфофеноловой кислотой с образованием тринитрофенола (пикриновая кислота), который в щелочной среде даёт жёлтую окраску за счёт образования тринитрофенолята калия (или натрия в зависимости от используемой щёлочи) в количестве, эквивалентном содержанию нитратов:
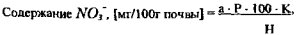
Интенсивность окраски определяют на фотоколориметре.
2.3.1. Ход анализа На технических весах взять 20 г свежей почвы, перенести в колбу объёмом 150-200 мл. Прилить цилиндром 100 мл дистиллированной воды (или 0.02 н. раствора K2SO4) и взболтать на ротаторе в течении 3 минут по песочным часам.
Отфильтровать в сухую посуду через воронку с двойным адПатым бумажным фильтром, стараясь перенести максимальное
С личество почвы на фильтр. Не следует наливать раствор в воронку 1/2 её объёма. Если фильтрат мутный, прибавить в колбу с почв0й 3-5 г активированного угля, либо отфильтровать до конца и добавить в фильтрат 0.4 мл 7%-го раствора щелочи и 0.6 мл 13%-го раствора AbCSOJj на 100 мл вытяжки. Выпавший осадок отфильтровать через чистый фильтр. Взять пипеткой 25-50 мл. прозрачного фильтрата в I фарфоровую чашку объёмом 50-100 мл и выпарить содержимое иа
водяной бане до 1 капли. При пересушивании сухого остатка могут быть потери нитратов. Снять чашку с водяной бани и осадок досушить на воздухе. В фарфоровую чашку после охлаждения прилить пипеткой 1 мл дисульфофеноловой кислоты и тщательно растереть сухой остаток небольшой стеклянной палочкой. Для удобства работы чашку следует поставить на специальную подставку . Прилить в чашку 10-15 мл дистиллированной воды, перемешать и опустить в раствор кусочек лакмусовой бумаги « 1 см2. Приливать из бюретки небольшими порциями 20%-ный раствор щёлочи до окрашивания лакмусовой бумаги в синий цвет.
При этом образуется комплексное соединение устойчивой жёлтой окраски. Если раствор помутнеет, добавить 2-3 капли щёлочи. Постоянно перемешивать стеклянной палочкой. Перенести количественно содержимое чашки в мерную колбу на 50 или 100 мл через небольшую воронку без фильтра. Довести раствор до метки, закрыть пробкой, взболтать. Раствор колориметрировать с синим светофильтром. Длина волны 400-440 нм.2.3.2. Расчёт

где: а - содержание нитратов по графику, мг, Р - разведение (100/Х), где X - количество (мл) исходного раствора, взятого для упаривания); К - коэффициент влажности почвы (учитывается только при анализе свежей почвы); Н * навеска свежей почвы, г; 100 - пересчет на 100 г почвы;
После этого можно рассчитать количество азота нитратов на ЮО г почвы:
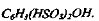
Построение калибровочного графика
Приготовление стандартного раствора: 1631 г перекристаллизованного KNO, растворить в дистиллированной воде в мерной колбе на 1 л.
Приготовление образцового раствора:
10 мл стандартного раствора перенести пипеткой в мерную колбу на 100 мл и довести дистиллированной водой до метки. В 1 мл полученного раствора содержится 0.01 мг NO, или 0.00226 мг N.
• В мерных колбах иа 50 или 100 мл приготовить стандартную шкалу в соответствии с таблицей, предварительно выпарив соответствующее количество образцового раствора. При выпаривании небольших количеств (1-5 мл) образцового раствора в чашку необходимо прилить 5-10 мл дистиллированной воды во избежание пересушивания сухого остатка. Окрашивание растворов калибровочной шкалы проводится в соответствии с описанной выше методикой.
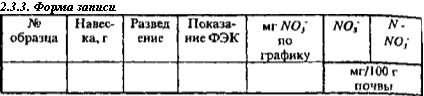
Таблица построения калибровочной шкапы для определения NO,
|
№ колбы |
1 |
2 |
3 |
4 |
5 |
6 |
7 _ |
|
кол-во образцового раствора,мл |
1 |
2 |
5 |
10 |
15 |
20 |
25 |
|
содержание NO; в колбе, мг |
0.01 |
0.02 |
0.05 |
0.10 |
0.15 |
0.20 |
0.25 |
? 3.5.
Реактивы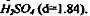 Дисульфофеноловая кислота - 74.6 г х.ч.
Дисульфофеноловая кислота - 74.6 г х.ч.
а осторожно смешать в толстостенной фарфоровой посуде с 500 концентрированной серной кислоты (d=1.84), постоянно
перемешивая фарфоровым шпателем или стеклянной палочкой. После того как смесь охладится до комнатной температуры, поместить её в круглую плоскодонную колбу объёмом 1 л, закрыть пробкой с обратным холодильником и нагревать на водяной бане 6-8 час. (до полного растворения фенола). Работу проводить под тягой! Можно также 50 г реактива фенол 2, 4 дисульфокислота растворить в 100 мл концентрированнойclass="lazyload" data-src="/files/uch_group52/uch_pgroup88/uch_uch225/image/28.jpg" alt="" /> 20%-й раствор NaOH или КОН. 20 г NaOH или КОН растворить в 80 мл дистиллированной воды. Лакмусовая бумага.
Еще по теме 2.3. Определение содержания нитратов в почве по Грандваль- Ляжу:
- Определения содержания нитратов в растительной продукции.
- Определение содержания питательных веществ в почве
- КОЛОРИМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ НИТРАТОВ И НИТРИТОВ (ПО Е. С. КОВАЛЕВОЙ, 1985)
- Определение нитратов в кормах, крови, молоке и патологическом материале с использованием реактива Грисса.
- ОПТИМИЗАЦИЯ СОДЕРЖАНИЯ МИКРОЭЛЕМЕНТОВ В ПОЧВЕ И ПРИМЕНЕНИЕ МИКРОУДОБРЕНИЙ
- Влияние бесподстилочного навоза на содержание углерода и азота в почве
- Содержание азота в почве и динамика его превращения
- РАСТЕНИЯ И СОДЕРЖАНИЕ В ПОЧВЕ ВАЖНЕЙШИХ ЭЛЕМЕНТОВ ПИТАНИЯ
- Определение соединений азота в почве, воде и кормах
- Определение обменного калия в почве.
- 2.4. Определение подвижных форм фосфорав почве
- Определение тяжелых металлов в почве, воде и кормах
- ОПРЕДЕЛЕНИЕ ВИТАМИНОВ В ПОЧВЕ-С ИСПОЛЬЗОВАНИЕМ ДРОЖЖЕЙ КАК ИНДИКАТОРОВ
- 2.2. Определение содержания аммонийного азота
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАЛЬЦИЯ (ГОСТ 17258-71)
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КАРОТИНА (ГОСТ 13496.17-95)
- ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ФОСФОРА (ГОСТ 26657-97)